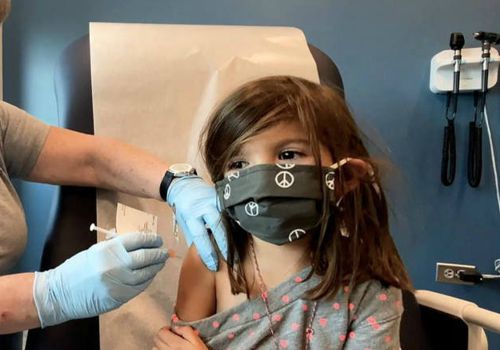
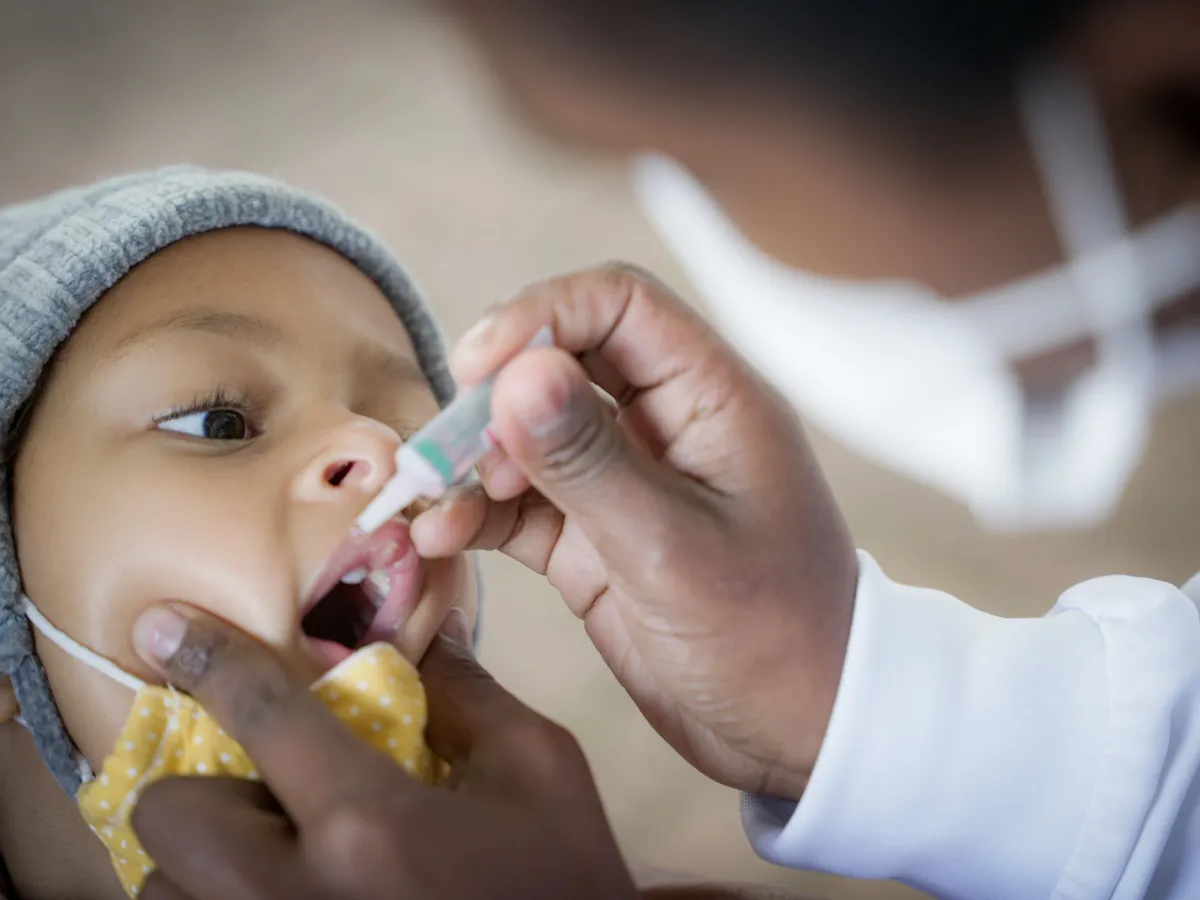
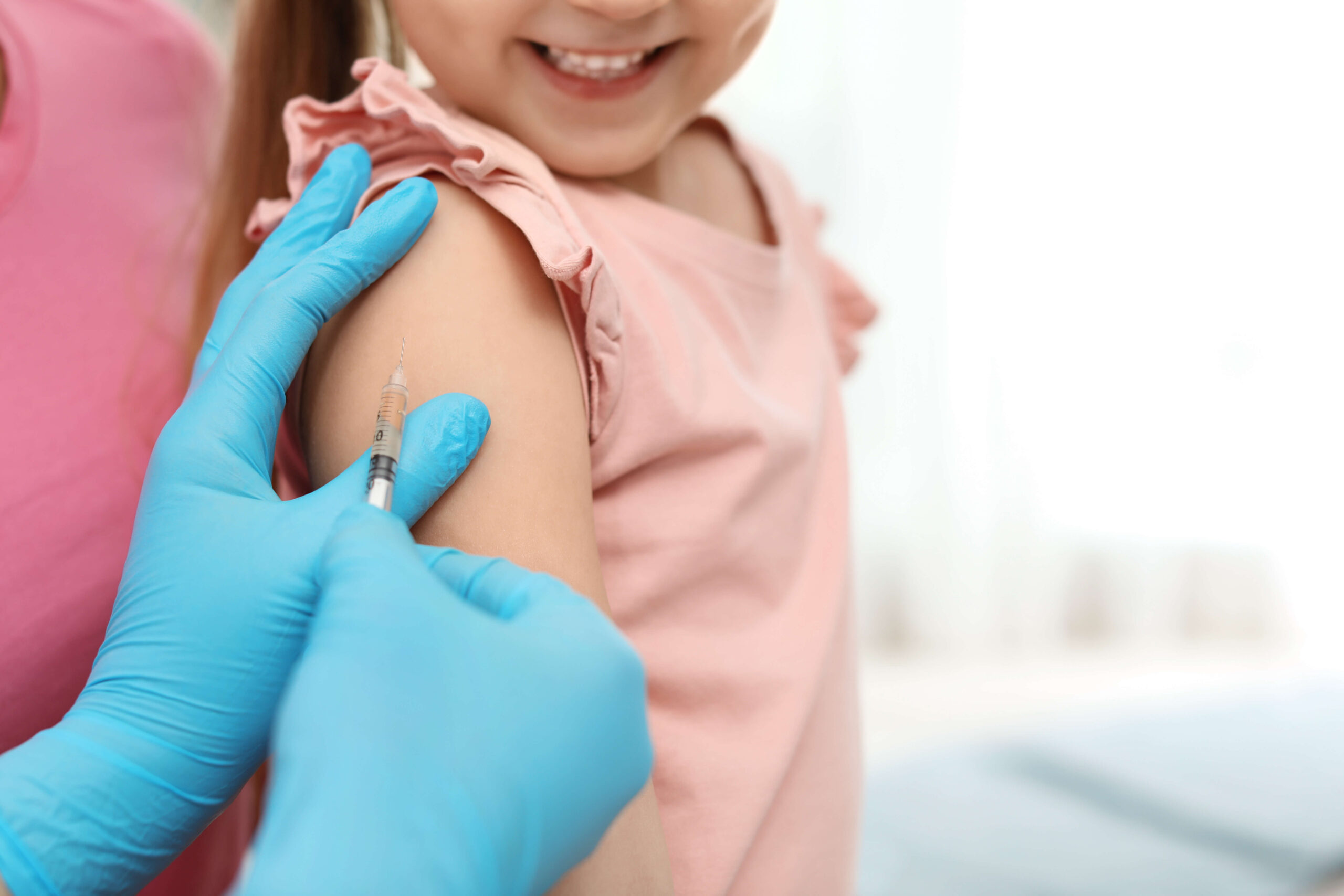
A ANVISA (Agência Nacional de Vigilância Sanitária) poderá autorizar a aplicação da vacina da Pfizer, contra a covid-19, em crianças de 5 a 11 anos. A área técnica do órgão se reúne nesta próxima quinta-feira (16), após terminar a análise do pedido da fabricante, para apresentar um relatório sobre a imunização desta faixa etária. Se ocorrer a liberação a decisão deverá ser publicada no D.O da União – Como a Pfizer já tem o registro definitivo da vacina no Brasil. Com a autorização da área técnica da Anvisa, a bula do imunizante será alterada para inclusão das crianças de 5 a 11 anos. O tema não necessitará de aprovação da diretoria colegiada.
O órgão recebeu a solicitação da Pfizer em 12 de novembro. Na ocasião, o laboratório submeteu à Anvisa dados e os estudos de segurança para embasar o pedido de vacinação de crianças. Além do corpo técnico da Agência, representantes de sociedades médicas brasileiras também participaram da análise do pedido da fabricante.
Ao pedir autorização à Anvisa, no mês passado, a Pfizer afirmou que a dosagem da vacina para a faixa etária seria ajustada e menor do que aquela aplicada em maiores de 12 anos. A proposta é ter frascos diferentes, com dosagem específica para cada grupo (maiores ou menores de 12 anos). Segundo a empresa, os frascos serão diferenciados pela cor.
A vacina da Pfizer está registrada no País desde 23 de fevereiro deste ano. Inicialmente, o imunizante foi autorizado para pessoas com mais de 16 anos. Em 11 de junho, a Anvisa liberou a inclusão da faixa etária de 12 a 15 anos.
Em agosto, a agência negou autorização para a aplicação do imunizante Coronavac contra a covid-19 em crianças e adolescentes de 3 a 17 anos. O pedido havia sido feito pelo Instituto Butantan, produtor da vacina no Brasil.
A decisão apontava que os dados apresentados pelo instituto não eram suficientes para comprovar a segurança da vacina no grupo pediátrico.
A vacina da Pfizer já está liberada nos Estados Unidos para crianças de 5 a 11 anos desde o dia 2 de novembro. Lá, a vacina é aplicada em duas doses com três semanas de intervalo. A dose foi ajustada para um terço por injeção em comparação com a aplicada em adultos e adolescentes. A aprovação da Agência de Medicamentos dos Estados Unidos (FDA), dizem especialistas, pesa favoravelmente para que o mesmo acontecesse no Brasil.